2026

#01 /FDA全面启动无预告突击检查早在2025年5月,美国食品药品监督管理局(FDA)便正式宣布扩大境外飞行检查范围,点名中国与印度为重点监管地区。自2026年5月起,FDA已彻底取消对中国工厂的...
2026
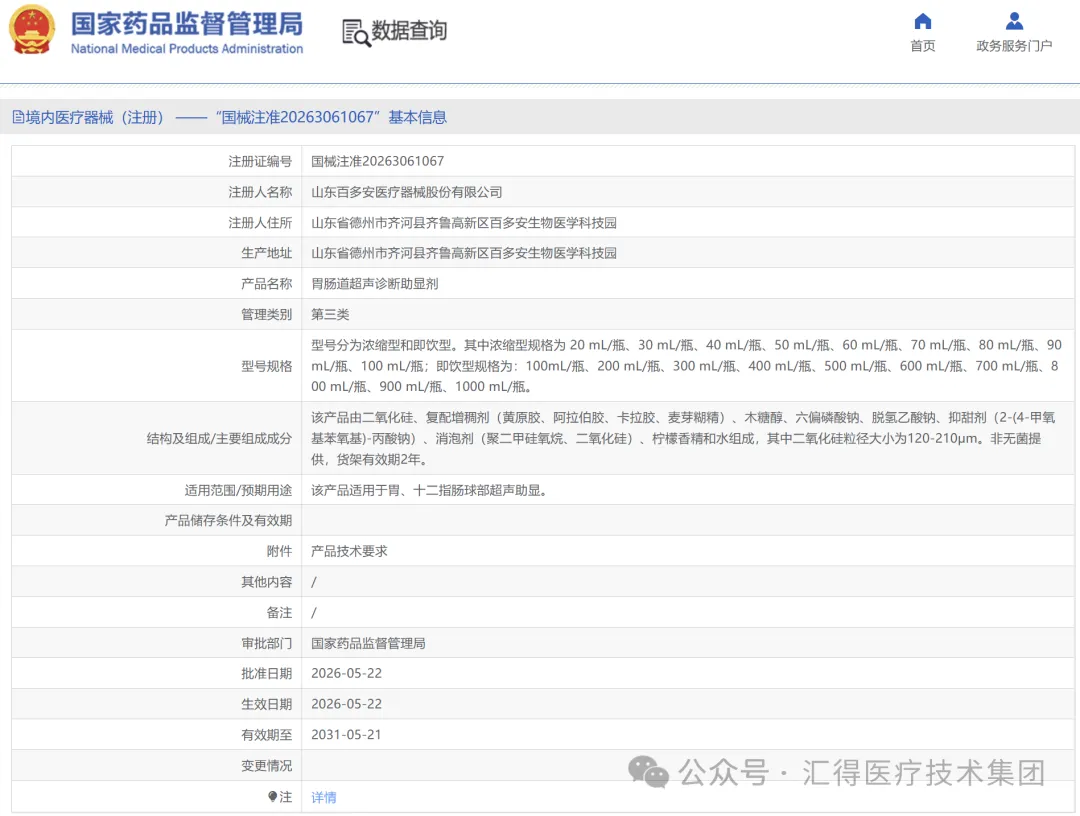
热烈祝贺,汇得医疗技术集团助力山东百多安医疗器械股份有限公司自主研发的【胃肠道超声诊断助显剂】产品成功获批国家药品监督管理局第三类医疗器械产品注册证,产品的持续安全性和有效性获得认可,自此可以在国内医...
2026

为深入贯彻落实创新驱动发展战略,推动创新科技成果从实验室到产业化的高效落地转化,广东行海生物科技有限公司与汇得医疗技术集团达成战略合作伙伴关系,双方将联合共建“创新产品合规与准入服务中心”,在医疗器械...
2026

近日,广西医疗器械行业协会副会长、秘书长、党支部书记莫凡带队,汇得医疗代表王珮力、吴俊随同,前往广西钦州开展医疗器械产业专项考察对接活动。本次考察聚焦推动政企医协深度联动、赋能钦州医疗器械产业高质量发...
2026

2026年3月13日,国家药监局、国家卫生健康委、国家医保局联合发布《关于做好后续品种实施医疗器械唯一标识工作的公告》(2026年第21号),正式敲定所有第二类、第一类医疗器械实施UDI的最终时间表。...
2026

汇得医疗的过去十年,是深耕积淀的1.0时代。集团构建了覆盖医疗器械全产业链的一站式专业技术服务能力,形成了快速响应客户需求的立体化区位布局。十年间累计服务超过5000家国内外医疗器械企业,助力客户获得...
2026

《医疗器械监督管理条例》(739 号令) 明确医疗器械监管主要的目的之一为保证医疗器械的安全有效,《医疗器械注册与备案管理办法》(47号令)要求医疗器械注册是对提交注册申请的医疗器械的安全性、有效...
2026

01图像扫描仪器(22-07-02)、图像分析仪器(22-07-03)等产品需符合的电气标准要求有哪些?是否要执行GB/T 42125.14-2023标准的要求? GB 4793.9-2013《测...
2026

医疗器械可用性,又称医疗器械的人因工程(Human Factors Engineering, HFE)或用户友好性,是确保医疗器械在实际使用环境中能够安全、有效、高效地被使用者操作的关键。随着技...
2026

01已注册医疗器械(体外诊断试剂)产品技术要求引用的强制性标准内容发生变化,何种情形下无需办理变更注册? 医疗器械(体外诊断试剂)注册证有效期内有新的强制性标准发布实施,已注册产品的注册证及其附件...
