2025

引言 金属骨针作为骨科手术中的关键植入器械之一,广泛应用于骨折固定、畸形矫正及关节融合等领域。近年来,随着材料科学和制造技术的进步,产业涌现出越来越多全新设计产品,金属骨针的设计逐渐从单一功能向精...
2025
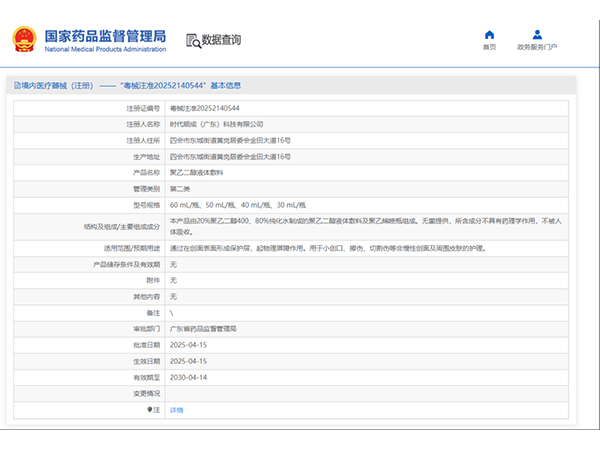
热烈祝贺,由我们汇得医疗CRO辅导合作的客户时代顺成(广东)科技有限公司自主研发的【聚乙二醇液体敷料】产品成功获批广东省药品监督管理局第二类医疗器械产品注册证,意味着该产品可以在国内医美医疗市场开启合...
2025
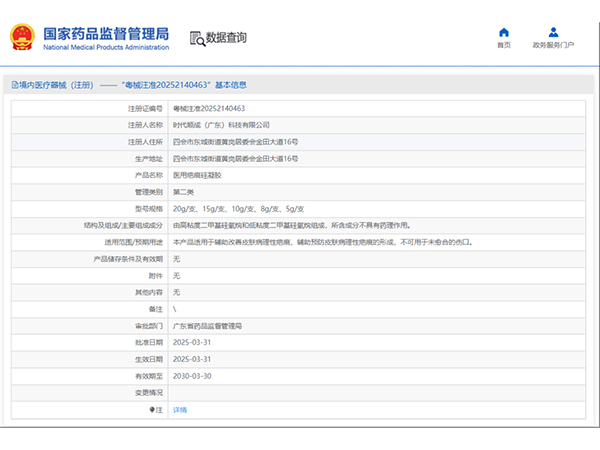
热烈祝贺,由我们汇得医疗CRO辅导合作的客户时代顺成(广东)科技有限公司自主研发的【医用疤痕硅凝胶】产品成功获批广东省药品监督管理局第二类医疗器械产品注册证,意味着该产品可以在国内医美医疗市场开启合...
2025

各省、自治区、直辖市和新疆生产建设兵团药品监督管理局,中国食品药品检定研究院,有关检验机构: 根据《国家药监局综合司关于开展2025年国家医疗器械质量抽查检验工作的通知》(药监综械管〔2025〕3号...
2025

01缝合针的概念 缝合针是外科手术中用于缝合人体或动物组织的医疗器械,由针体和针眼(或针尾)组成,通常与缝合线配合使用。其设计需满足穿透力强、操作灵活、减少组织损伤等要求,材质以...
2025

01目的 为规范对医疗器械不合格品的管理,防止不合格医疗器械流入市场,确保医疗器械的质量和使用安全,特制定本程序。02适用范围 本工作程序适用于本公司经营的所有医疗器械不合格品的处理过程,包括...
2025

2023年1月27日,FDA和加拿大卫生部共同启动eSTAR试点工作。2023年6月9日,eSTAR系统开放,可用于向CDRH提交Pre-submission。自2023年10月1日起,除非获得豁免...
2025

01什么是ISO三体系认证?ISO三体系认证是指:ISO9001认证、ISO14001认证、ISO45001认证。ISO9001是国际标准化组织(ISO)制定的质量管理体系标准。ISO14001是国际...
2025

按照《医疗器械注册与备案管理办法》、《体外诊断试剂注册与备案管理办法》的要求,申请注册或者进行备案提交的医疗器械产品检验报告可以是申请人、备案人的自检报告,也可以是委托有资质的医疗器械检验机构出具...
2025

01手术膜的概念 手术膜是一种医用薄膜,用于手术时覆盖在手术部位,以防止手术区域污染和感染。手术膜通常由聚丙烯或聚乙烯等材料制成,具有防水、防血液渗透和防细菌感染等特性。02手术膜的分类 根据《医...
